Theo Lenharo, M. (2024). Move over, CRISPR: RNA-editing therapies pick up steam. Nature, 626(8001), 933–934. https://doi.org/10.1038/d41586-024-00275-6
Chỉnh sửa RNA từ lâu đã được cho là liệu pháp thay thế an toàn và linh hoạt hơn các kỹ thuật chỉnh sửa DNA như CRISPR, nhưng đồng thời nó cũng đặt ra những vấn đề kỹ thuật phức tạp hơn. Sau hàng thập kỷ nghiên cứu về liệu pháp chỉnh sửa phân tử RNA, đã có ít nhất ba liệu pháp chỉnh sửa RNA được đưa vào thử nghiệm lâm sàng. Đây là những bước tiến lớn trong việc nghiên cứu chỉnh sửa RNA.
Trong 1 năm gần đây, đã có hai liệu pháp chỉnh sửa RNA điều trị các bệnh di truyền được phê duyệt để thử nghiệm lâm sàng, tạo thêm hy vọng để nhân loại có liệu pháp điều trị an toàn các căn bệnh này.
    |
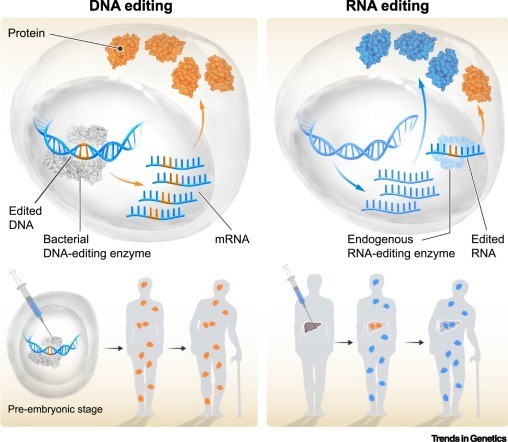 |
| Hình 1. So sánh hiệu quả của phương pháp chỉnh sửa DNA và RNA |
Công việc trước mắt
RNA có vai trò quan trọng trong quá trình tổng hợp protein: thông tin di truyền từ DNA được phiên mã thành RNA thông tin (mRNA) trước khi được dịch mã thành protein.
Không giống như chỉnh sửa DNA bằng CRISPR, chỉnh sửa RNA không làm biến đổi gen. Nó cũng không gây ra những thay đổi vĩnh viễn so với chỉnh sửa DNA, bởi vì sự tồn tại của các phân tử RNA là tạm thời. Điều này mang lại lợi thế so với rủi ro của liệu pháp CRISPR chỉnh sửa DNA với các lo ngại về tác dụng không mong muốn (off-target) có thể chỉnh sửa cả các trình tự nằm ngoài vùng gen mục tiêu.
Chỉnh sửa Nucleotide đơn
Phương pháp chỉnh sửa RNA phổ biến là chỉnh sửa từng Nucleotide đơn bằng cách tận dụng một enzyme đã có sẵn trong tế bào: Adenosine deaminase tác động RNA (adenosine deaminase acting on RNA - ADAR). Enzyme này hoán đổi Adenin trong trình tự RNA thành Inosin.
    |
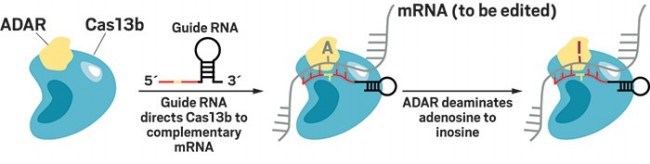 |
| Hình 2. Phương pháp chỉnh sửa Adenin thành Inosin trong trình tự RNA nhờ enzyme Adenosine deaminase (Science 2017, DOI: 10.1126/science.aaq0180). |
Adenosine deaminase (Science 2017, DOI: 10.1126/science.aaq0180).
Công ty Wave Life Sciences ở Cambridge, Massachusetts, đang nghiên cứu chỉnh sửa đơn bazơ để điều trị bệnh rối loạn di truyền thiếu alpha-1 antitrypsin (AATD) gây tổn hại cho phổi và gan. Bệnh này làm giảm sản sinh AAT, một protein được tạo ra trong tế bào gan, bảo vệ phổi khỏi tổn thương do hít phải không khí ô nhiễm hoặc các yếu tố kích thích khác. Thử nghiệm lâm sàng thuốc của công ty đã bắt đầu vào tháng 12 năm ngoái tại Anh và Úc, và sẽ tiếp tục đánh giá tính an toàn và các đặc điểm khác của thuốc.
Sản phẩm của Wave là một chuỗi ngắn nucleotit có thể hướng các enzyme ADAR có sẵn trong cơ thể thay đổi một nucleotit cụ thể trong mỗi phân tử mRNA, nhằm sửa chữa đột biến ảnh hưởng đến sản xuất AAT. Paul Bolno - chủ tịch và giám đốc điều hành của Wave nói: “Bằng cách sử dụng cơ chế nội sinh của tế bào để chỉnh sửa đơn base, bạn có thể tạo ra một protein bình thường. Và chúng tôi đã chứng minh được rằng protein đó có thể được biểu hiện ở mức cao. Ở chuột, thuốc này đã chỉnh sửa khoảng 50% mRNA mục tiêu trong tế bào gan, đủ để tạo ra hiệu quả điều trị.”
Chỉnh sửa toàn bộ đoạn exon
Một liệu pháp khác, gọi là chỉnh sửa RNA exon, có thể thay đổi hàng nghìn Nucleotide trong một phân tử RNA cùng một lúc. “Chỉnh sửa exon giống như chỉnh sửa một đoạn văn thay vì chỉnh sửa một lỗi chính tả”. Công nghệ này đặc biệt thích hợp đối với các bệnh rối loạn trong đổi chất do nhiều đột biến trong gen gây ra.
Kỹ thuật này nhắm đến pre-mRNA, được phiên mã từ DNA và sau đó được xử lý để tạo ra mRNA. Pre-mRNA bao gồm cả exon - những phần RNA mang thông tin mã hoá để tổng hợp protein, và intron - nhưng thông tin mã hoá. Qua cơ chế cắt nối RNA, các intron được cắt ra khỏi pre-mRNA, và các exon được ghép lại với nhau để tạo thành mRNA trưởng thành và được dịch mã thành protein.
    |
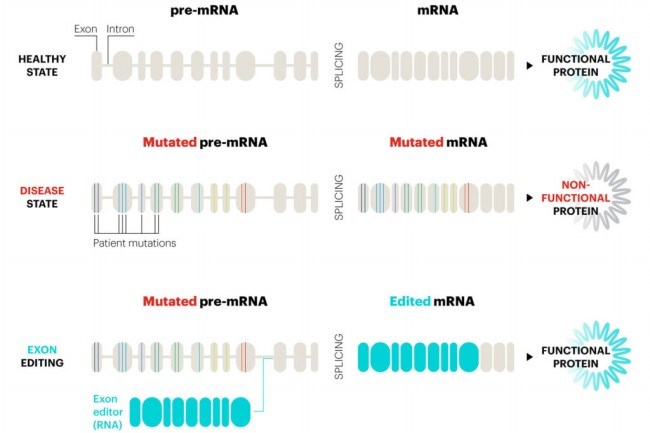 |
| Hình 3. Phương pháp chỉnh sửa RNA exon của Ascidian Therapeutics |
Nhiều công ty tham gia phát triển liệu pháp này, ví dụ như Công ty Ascidian Therapeutics ở Boston, Massachusetts, đang tận dụng quá trình cắt nối RNA để loại bỏ các exon chứa đột biến và thay thế chúng bằng những exon khỏe mạnh. Tháng trước, Ascidian Therapeutics đã nhận được sự chấp thuận của Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ cho phép thử nghiệm lâm sàng việc chỉnh sửa exon để điều trị bệnh Stargardt gây mất thị lực. Những người bị bệnh này có nhiều đột biến trong một gen, dẫn đến thiếu một loại protein giúp bảo vệ võng mạc. Phương pháp này sử dụng đoạn DNA được thiết kế nhân tạo và chuyển vào tế bào giúp tạo ra các exon RNA bình thường. Chúng sẽ thay thế các exon đột biến trong quá trình cắt nối pre-mRNA, tạo ra các protein chức năng. Đoạn DNA này cũng tạo ra các chuỗi RNA hỗ trợ việc chỉnh sửa exon. Nhà sinh vật học Robert Bell, người đứng đầu nghiên cứu tại Ascidian cho biết: “Với một phân tử, liệu pháp này có thể thay thế 22 exon cùng một lúc”.
RNA tiêu diệt ung thư
Tiềm năng của liệu pháp chỉnh sửa RNA không chỉ giới hạn ở các bệnh di truyền. Rznomics, một công ty sinh dược ở Seongnam, Hàn Quốc, đang thử nghiệm một trình chỉnh sửa RNA để điều trị loại ung thư gan phổ biến nhất: ung thư biểu mô tế bào gan (hepatocellular carcinoma). Từ tháng 9/2022, công ty này đã bắt đầu một thử nghiệm lâm sàng ở Hàn Quốc.
Phương pháp của Rznomics liên quan đến cắt nối mRNA nhưng khác với liệu pháp của Ascidian, nó không sử dụng cơ chế cắt nối có sẵn của tế bào. Thay vào đó, công ty đã sử dụng một ribozyme tự nhiên, đây là một phân tử RNA có khả năng cắt nối các trình tự của mRNA. Các nhà nghiên cứu đã thiết kế ribozyme giúp cắt mở các mRNA trong tế bào ung thư và chèn vào “một món hàng chết người”, đó là một chuỗi RNA khi được dịch mã thành protein thì sẽ tổng hợp chất độc gây ra sự tự chết tế bào (apoptosis). Khi các tế bào ung thư xung quanh tiếp xúc với tế bào này, chất độc sẽ lan truyền và thúc đẩy sự tự chết. Liệu pháp phân tử này thay thế một chuỗi RNA liên quan đến sự phát triển khối u.
CLB Bio-Sciencenews, Khoa Công nghệ sinh học